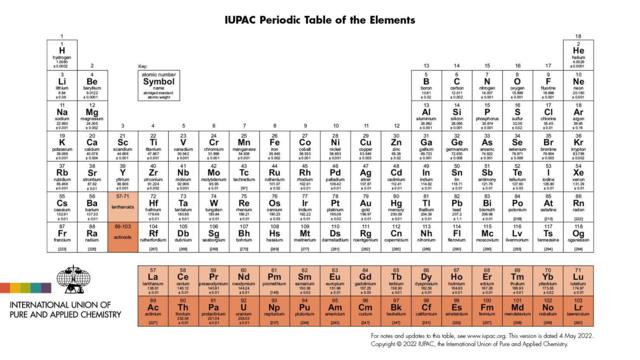
Автор фото, AFP via Getty Images
Последний периодическая таблица элементов обновлялась десять лет назад. Свое место в ней нашли элементы 113, 115, 117 и 118. А международный надзорный орган в области химии решился на уникальный шаг: назвал один из элементов в честь живого физика.
Юрий Оганесян возглавил российско-американскую исследовательскую группу, открывшую элемент 118 (оганессон) в 2002 году. Потребовались годы, чтобы подтвердить результаты, – элемент настолько радиоактивен, что было создано лишь несколько атомов.
Можно задаться вопросом: почему за 10 лет с тех пор не добавили ни одного нового элемента, и можно ли когда-нибудь считать периодическую таблицу завершенной? Что такое периодическая таблица
Периодическая таблица — это, в сущности, карта химических элементов с множеством квадратов, заполненных их химическими веществами. Ее постоянно перерисовывают.
Элемент — это чистое вещество, состоящее из одного типа атомов. Атомы являются основными строительными блоками материи и имеют ядро, обычно содержащее положительно заряженные протоны и незаряженные нейтроны, окруженное отрицательно заряженными электронами. Из частей периодической таблицы состоит все, что мы знаем во Вселенной, включая самих.
Еще в начале 1800-х годов открыли многие элементы, но они не были систематизированы. Несколько ученых стремились поменять это.
Одним из них был британский химик Джон Ньюлендс. Он упорядочил элементы по атомному весу (мере веса атома) и увидел, что каждый восьмой имеет подобные свойства. Например, литий, натрий и калий расположены по восьми позициям друг от друга и демонстрируют схожие реакции с водой. Он назвал это законом октау. Российский химик Дмитрий Менделеев, которого называют отцом периодической таблицы, взял идею повторяющихся свойств и сформулировал ее в так называемый период.
В 1869 году он создал основу для современной периодической таблицы, упорядочив элементы по атомному весу. В отличие от версии Ньюлендса, в его таблице оставались пробелы для недостающих элементов. Его работа приобрела популярность, когда эти предусмотренные ученым элементы были позже открыты.
Сегодня элементы периодической таблицы определяются и организуются по их атомному номеру – количеству протонов в ядре. Водород имеет один протон, тогда как оганесон – 118.
Элементы в одном столбце обладают схожими химическими свойствами, например, как они реагируют с другими веществами.
Они часто имеют определенную закономерность в своих физических свойствах, таких как температура плавления, что помогает ученым предсказать их поведение. Инженеры, например, могут использовать периодическую таблицу для выбора материалов при проектировании мостов и самолетов. Если ученый считает, что он открыл новый элемент, глобальный надзорный орган, который называется Международный союз чистой и прикладной химии (IUPAC), проверяет его существование, а элемент получает место в таблице. Этот процесс может занять годы.
Считается, что мы нашли все природные элементы на Земле, и они составляют большую часть таблицы. Более тяжелые элементы могут быть созданы искусственно в лаборатории путем сочетания двух более легких.
Благодаря развитию технологий, ученые смогли добавить в таблицу больше сверхтяжелых элементов. Теоретически люди могли бы продолжать пытаться создавать новые элементы, но это становится все сложнее.
Создание новых элементов
Чтобы соединить более легкие элементы вместе для создания все более тяжелых новых, “мы должны привлекать все больше энергии, строя все большие циклотроны или ускорители”, объясняет профессор Фил Блоуэр, руководитель кафедры химии.
“Поскольку элементы становятся все больше и тяжелее, они становятся все менее стабильными из-за протонов в ядре”, – говорит Блоуэр.

Автор фото, San Francisco Chronicle/Hearst Newspapers via Getty Images
Соотношение протонов и нейтронов в ядре определяет, будет ли ядро стабильным или нестабильным. Положительно заряженные протоны естественным образом отталкиваются друг от друга, но присутствие нейтронов может удерживать их вместе.
“Когда вы создаете все более тяжелые и тяжелые элементы, вы добавляете больше протонов к ядру, и чтобы оно не распалось, вам нужно растущее количество нейтронов”, – объясняет доктор Чинция Имберти, руководитель группы Imaging Metallomics в Королевском колледже Лондона.
Элемент может существовать с разным количеством нейтронов – эти вариации называются изотопами. Нестабильные изотопы радиоактивны – они распадаются, излучая радиацию.
Автор фото, KTSDESIGN/Science Photo Library via Getty Images
“Все элементы тяжелее свинца (элемент 82), являются радиоактивными, они по своей сути нестабильны и разлагаются”, – пояснит. Кардифф и почетный профессор Университета Уорвика в Великобритании.
“Если бы мы смогли создать один атом одного из этих элементов, он бы недолго просуществовал”, – объясняет он.
Это особенно относится к элементам, начиная с номера 100 (фермий) и далее.
“Вы создаете несколько атомов, и можете немного знать об их физических свойствах. Но они не имеют никакого практического применения”, – объясняет доктор Имберти.
Тем не менее, поиски следующих элементов, которые добавили бы в периодическую таблицу новую строчку, продолжаются. Многие попытки найти числа 119 и 120 пока не увенчались успехом, но разные исследовательские группы продолжают попытки.
Ученые говорят, что исследование элементов на крайних уровнях может дать нам новое понимание того, как работают атомы, границы атомных ядер и возможность проверить теории ядерной физики.
“Нужно думать не только о том, сможем ли мы это создать, – говорит Имберти, – но и о том, сможет ли оно прожить достаточно долго, чтобы мы могли открыть его в осмысленном смысле, узнать немного о нем… Прежде чем оно исчезнет”.







