Автор фото, Emmanuel Lafont/BBC
После почти 100 лет разработок методы лечения, усиливающие иммунную систему организма для борьбы с раком, достигают расцвета – и спасают жизнь пациентов.
Когда 71-летнюю Морин Сидерис лечили от рака толстой кишки в 2008 году, ей пришлось лечь под нож. Лечение было успешным, но послеоперационное восстановление оказалось изнурительным. Через четырнадцать лет у Сидерис, живущей в Нью-Йорке, диагностировали рак пищевода – и на этот раз лечение, предложенное в рамках клинического испытания, выглядело радикально иначе.
Каждые три недели она приезжала в онкологический центр Memorial Sloan Kettering в Нью-Йорке на 45-минутную инфузию препарата под названием достарлимаб. Уже через четыре месяца лечения опухоль Сидерис исчезла – без операции, химиотерапии или облучения, а единственным серьезным побочным эффектом стала надпочечница, вызывающая усталость.
“Это невероятно, – говорит она. – Почти как научная фантастика”.
Однако это – реальность.
Сидерис – одна из все большего числа пациентов, которых лечат от рака с помощью иммунотерапии – метода лечения, который после более чем столетия развития начинает работать в полную силу. Вместе с ним появляется надежда на персонализированную терапию, длительную ремиссию и меньшее количество побочных эффектов по сравнению с другими методами, такими как химиотерапия и лучевая терапия.
“У меня перехватывает дыхание и появляются мурашки по коже”, – говорит Дженнифер Варго, профессор хирургической онкологии и исследовательница иммунотерапии в онкологическом центре MD Anderson в Техасе.
“Люди живут и живут с высоким качеством жизни. Мы говорим о излечении”, – добавляет она.
Организм обладает природной способностью “обнаруживать и уничтожать клетки, которые выглядят как” чужеродные “”, объясняет Карен Кнудсен, исполнительный директор Института иммунотерапии рака Паркер – американской некоммерческой организации, способствующей развитию иммунотерапии.
Если система работает должным образом, это должно относиться и к клеткам, которые стали раковыми.
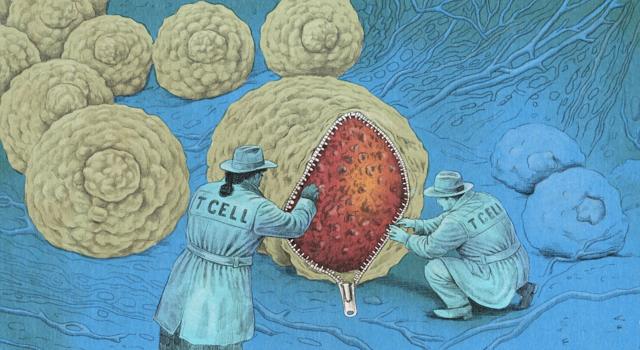
Но иногда раковые клетки избегают или перехитривают эту систему, что приводит к опасному неконтролируемому росту. Они прячутся на виду, потому что их невозможно отличить от здоровых клеток вокруг.
Цель иммунотерапии – сорвать эту маску, чтобы иммунная система увидела раковые клетки такими, какие они есть. Она усиливает защитные механизмы иммунитета, чтобы тот мог находить и уничтожать злокачественные клетки – с потенциально поразительными результатами.
Как иммунотерапия борется с раком сегодня
Двумя известными формами иммунотерапии являются CAR‑T‑клеточная терапия и ингибиторы иммунных контрольных точек.
CAR-T-клеточная терапия предусматривает извлечение Т-клеток (высокоспецифических иммунных клеток, выслеживающих и уничтожающих определенных чужеродных захватчиков) из крови пациента, их модификацию в лаборатории таким образом, чтобы они могли находить и атаковать раковые клетки, а затем возвращение этих “сил”. В настоящее время такие методы применяются для лечения раков крови.
Ингибиторы иммунных контрольных точек – это препараты, которые выключают встроенный “выключатель” иммунной системы. Этот предохранитель имеет важную функцию – он не позволяет чрезмерно агрессивным иммунным реакциям повреждать здоровые клетки. Однако некоторые раковые клетки могут включить этот выключатель, заставляя Т-клетки отступить и таким образом избежать обнаружения. Ингибиторы контрольных точек предотвращают это, поэтому Т-клетки распознают раковые клетки как угрозу и начинают атаку.
Ученые, заложившие основу этой инновации, получили Нобелевскую премию в 2018 году, и сегодня эти препараты применяют при многих видах рака.
Впрочем, оба подхода имеют ограничение. Хотя исследования продолжаются, ученым было сложно заставить CAR-T-клеточную терапию эффективно работать против твердых опухолей (в отличие от раков крови), на которые приходится более 90% новых диагнозов. К тому же это лечение дорогостоящее и трудоемкое в применении.
Автор фото, Emmanuel Lafont/BBC
Ингибиторы иммунных контрольных точек, в свою очередь, могут сопровождаться “калейдоскопом побочных эффектов”, говорит Самра Турайлич, онкологиня из Института Фрэнсиса Крика в Лондоне.
Дело в том, что выключатели иммунной системы предназначены для того, чтобы не позволять организму атаковать собственные ткани, а устранение этой защиты может поставить под угрозу не только опухоли, но и нераковые клетки.
По данным Национального института рака США, распространенные побочные эффекты включают кожную сыпь, диарею и усталость, а в редких случаях возможно воспаление печени, сердца и почек. Такой компромисс может быть оправданным, если препарат контролирует агрессивный рак. Но это бывает не всегда.
Большая проблема для всей онкологии, по словам Турайлича, заключается в том, что ни одна иммунотерапия не работает у 100% пациентов. Причин может быть много – от структуры опухоли, уменьшающей ее доступность для иммунной системы, до характеристик самих иммунных клеток. В общем, на иммунотерапию соответствуют примерно от 20% до 40% пациентов.
Это означает, что многие люди – фактически большинство – подвергаются побочным эффектам, не говоря уже о потерянном времени и надежде, без пользы.
Многовекторные подходы
Как сделать так, чтобы больше пациентов получали пользу от иммунотерапии? Исследователи подходят к этой проблеме со многих сторон.
Исследования Варго, хотя и предыдущие, свидетельствуют, что пациенты, соблюдающие диету с высоким содержанием клетчатки, могут иметь лучшие результаты благодаря изменениям в кишечном микробиоме, которые могут влиять и на иммунную систему, и на опухоль.
Другие неожиданные исследования показывают, что статины – недорогие и доступные препараты для снижения уровня холестерина – могут усиливать эффект иммунотерапии из-за неожиданных изменений в клеточной коммуникации.
Может иметь значение даже время лечения: некоторые недавние исследования намекают, что пациенты, получающие лечение в ранние часы, имеют лучшие результаты, чем те, кого лечат позже.
Еще одним способом повысить эффективность может быть сочетание иммунотерапии с другими методами лечения рака, такими как лучевая терапия или ультразвук.
“Облучение на самом деле может сделать опухоль видимой для иммунной системы”, – объясняет Сандра Демария из медицинского центра Weill Cornell, которая исследовала этот комбинированный подход.
Ультразвуковая терапия, использующая высокочастотные звуковые волны для атаки опухолей, может действовать подобно.
Другие исследователи используют способность иммунотерапии к индивидуализации, тщательно подбирая для пациентов лучшее возможное лечение.
Персонализированная медицина вызывает энтузиазм во многих областях, но Кнудсен подчеркивает, что для онкологии она особенно важна, учитывая разнообразие заболевания.
“Рак – это не одна болезнь, – говорит Кнудсен. – Это 200 различных болезней, которые возникают по разным причинам и нуждаются в разном лечении”.
Даже у двух пациентов с одинаковым типом и стадией рака болезнь на клеточном уровне может быть разной.
“Отрасль находится в точке перелома, – говорит Демария. – Мы можем перейти к лечению не рака, а конкретного пациента”.
Ученые из Memorial Sloan Kettering Cancer Center уже опробовали одну многообещающую стратегию, основанную на открытии, что опухоли с определенным генетическим профилем хорошо реагируют на ингибиторы иммунных контрольных точек, такие как достарлимаб. В двух небольших исследованиях 2022 и 2024 годов, посвященных лечению рака прямой кишки с таким профилем, терапия полностью уничтожила опухоли.
Впоследствии команда расширила исследования, охватив 117 пациентов с различными типами опухолей – в частности раком пищевода, мочевого пузыря и желудка – которые имели ту же генетическую подпись. Из 103 человек, которые завершили полный курс лечения, у 84, включая Сидерис, опухоли полностью исчезли; только двоим понадобилась дополнительная операция.
Исследователи из MD Anderson сообщили о подобных результатах для подхода с использованием другого ингибитора контрольных точек. Другие группы также показали, что даже если пациентам в конце концов все же делают операцию, их хирургические результаты могут быть лучше, по крайней мере в некоторых случаях, если опухоли сначала атакуют иммунотерапией.
Хотя требуются дальнейшие исследования, такие результаты обнадеживающие, поскольку они открывают путь к менее инвазивной, но высокоэффективной эре лечения, говорит Луис Диас, руководитель направления опухолей в онкологическом отделении Memorial Sloan Kettering.
“Мы должны перейти от средневековья к современности, – говорит он. – Удалять прямую кишку, желудок или мочевой пузырь – мы должны делать лучше, чем это”.
Оговорка состоит в том, что только около 5% опухолей имеют генетический состав, который делает их пригодными для безоперационного иммунотерапевтического лечения, которое изучали Диас и его коллеги.
“Для остальных 95% нужно что-то столь же эффективное”, – говорит он.
Обещание противораковых вакцин
С этой целью исследователи продолжают искать новые подходы к иммунотерапии и совершенствовать старые – в частности, противораковые вакцины.
Традиционные вакцины знакомят организм с частями патогена, например вируса, чтобы он мог “потренироваться” формировать иммунный ответ на подлинную угрозу. Подобная концепция может работать и для рака, говорит Кнудсен, но ее можно использовать для лечения, а не для профилактики.
Автор фото, Emmanuel Lafont/BBC
Раковые клетки покрыты разнообразными поверхностными белками. Используя вакцинные технологии, исследователи могут научить иммунную систему пациента распознавать и атаковать эти белки, запуская мощный ответ против конкретного рака, объясняет Кнудсен.
Уже есть предварительные доказательства поддержки этого подхода. Исследователи из онкологического института Dana-Farber в США недавно создали персонализированные вакцины для девяти человек с одним типом рака почки. После хирургического удаления опухолей пациентов вакцинировали, чтобы избавиться от любых остаточных опухолевых клеток в организме. В исследовании, опубликованном в 2025 году, команда сообщила, что все девять пациентов сформировали целевой противораковый иммунный ответ и не имели признаков рака спустя годы после операции.
Персонализированные вакцины также продемонстрировали перспективность лечения меланомы.
“Это смелый новый мир, – говорит Кнудсен. – Это и есть определение прецизионной медицины. Теперь мы, возможно, сможем очень быстро разрабатывать вакцинальные стратегии против именно той опухоли, которая у вас есть”.
Несмотря на этот энтузиазм, предстоит еще долгий путь. Требуются дополнительные исследования, чтобы подтвердить некоторые изучающие сейчас обнадеживающие методы и приблизиться к будущему, в котором врачи смогут точно и надежно подбирать пациентам лечение, которое будет работать против их конкретного рака.
“Было много очень перспективных мишеней и новых препаратов, которые не прошли дальше ранних фаз клинических испытаний”, – предостерегает Демария.
Возможно, определенная подгруппа пациентов не будет реагировать ни на один вид иммунотерапии, говорит Диас. Разные раки имеют разные “суперспособности”, позволяющие им расти и преуспевать, и иммунная система является лучшим противником для одних, чем для других.
Но для пациентов, отвечающих на лечение, иммунотерапия уже доказывает, что она не только спасает жизнь, но и изменяет ее.
Сидерис, пациентка из Нью-Йорка, участвовавшая в испытании Диаса, чувствует себя частью более светлого будущего онкологии.
“Мы двигаемся в таком замечательном направлении, – говорит она. – Один из врачей сказал мне, что через 10 лет любая химиотерапия и облучение будут выглядеть как кровопускание – настолько это будет устарело”.







